トピロキソスタットの副作用と効果について
トピロキソスタットの作用機序と薬理学的特性
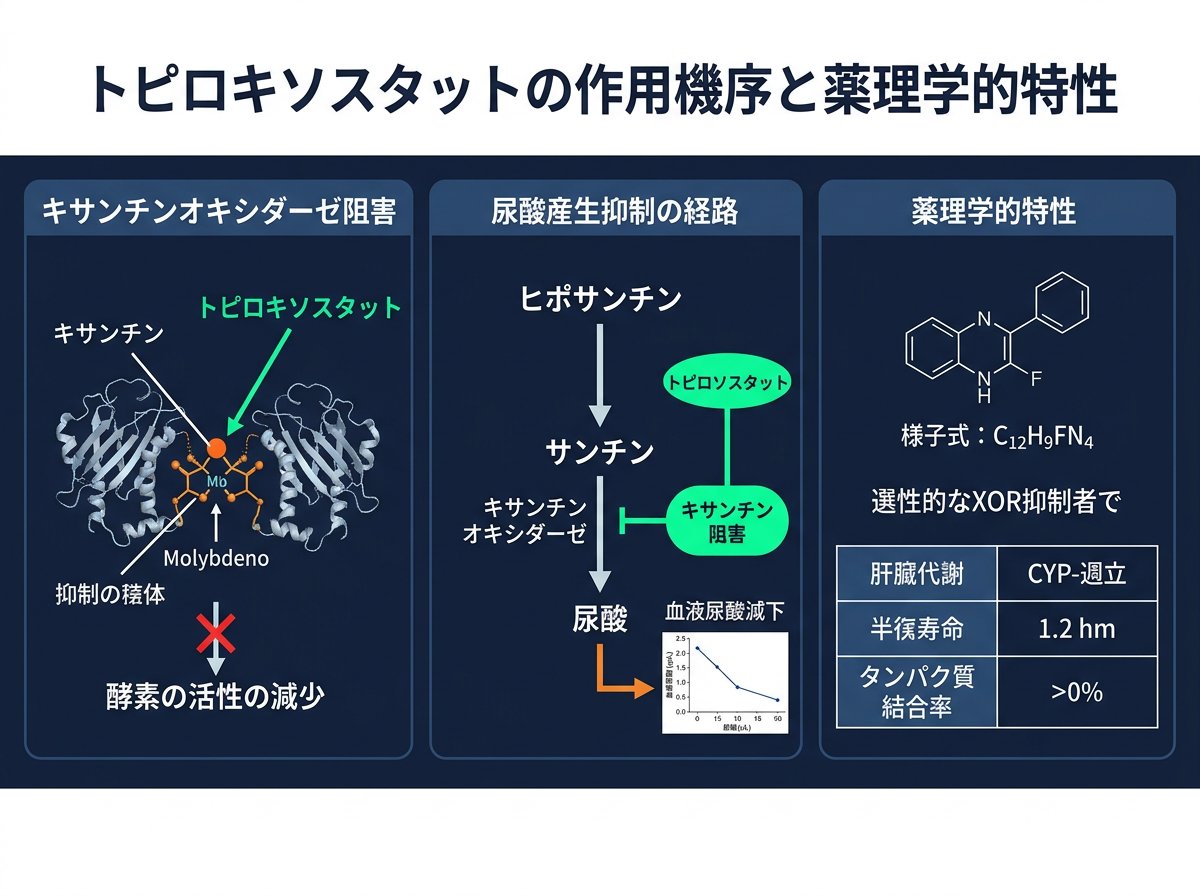
トピロキソスタットは、非プリン型の選択的キサンチン酸化還元酵素(XOR)阻害剤として開発された高尿酸血症治療薬です。従来のアロプリノールとは異なり、プリン骨格を持たない化学構造が特徴で、より選択的にXORを阻害することができます。
XORは生体内でヒポキサンチンからキサンチン、そしてキサンチンから尿酸への変換を触媒する酵素です。トピロキソスタットはこの酵素に競合的に結合し、阻害することで尿酸の生成を抑制します。具体的には、XORに対するKi値(阻害定数)は5.1nmol/Lと非常に低く、強力な阻害作用を示します。
トピロキソスタットの薬理学的特性として注目すべき点は以下の通りです。
- 選択性の高さ - 他のプリン・ピリミジン代謝酵素には影響せず、XORに特異的に作用
- 二重の作用 - 尿酸生成抑制に加え、尿中尿酸排泄量も低下させる作用がある
- 用量依存性 - 40mg/日から開始し、段階的に80mg/日、最大120mg/日まで増量可能
- 血中濃度 - 服用後約1時間で最高血中濃度に達し、半減期は約5時間
チンパンジーを用いた高尿酸血症モデルの実験では、トピロキソスタット単回経口投与により尿中への尿酸排泄量が有意に低下したことが確認されています。この特性は、高尿酸血症の治療において尿酸生成を抑制しながら、同時に尿路への負担も軽減できる可能性を示唆しています。
トピロキソスタットの主な副作用と発現頻度
トピロキソスタットは比較的安全性の高い薬剤ですが、様々な副作用が報告されています。国内で実施された臨床試験では、826例中292例(35.4%)に臨床検査値異常を含む副作用が認められました。使用成績調査(市販後調査)では4,329例中301例(6.95%)に副作用が発現しており、副作用の発現率は臨床試験よりも低い傾向にありました。
主な副作用とその発現頻度:
| 副作用カテゴリ | 主な症状 | 発現頻度 | 発現時期 |
|---|---|---|---|
| 肝機能障害 | AST・ALT上昇 | 2.9%(重篤なものは0.2%) | 投与開始2-4週後 |
| 痛風関節炎 | 関節の痛み・腫れ | 10.0% | 投与開始直後〜数週間 |
| 腎機能関連 | 尿中α1ミクログロブリン増加、β2ミクログロブリン増加 | 20.7〜27.3% | 投与開始後数週間〜 |
| 皮膚障害 | 多形紅斑、そう痒症 | 0.5%未満(多形紅斑)、0.35%(そう痒症) | 投与後2-8週間 |
| 消化器症状 | 口内炎、下痢、悪心、腹部不快感 | 1%未満 | 投与初期 |
特に注目すべき重大な副作用は肝機能障害と多形紅斑です。肝機能障害は比較的高頻度(2.9%)に発現し、AST・ALT値の上昇を伴います。重篤な肝機能障害の発現率は0.2%と報告されており、定期的な肝機能検査による経過観察が推奨されています。
また、長期投与試験では尿中微量タンパク(α1ミクログロブリン、β2ミクログロブリン)の増加が20%以上の高頻度で認められており、腎機能への影響についても注意が必要です。
投与開始初期には痛風関節炎(痛風発作)の発現リスクが増加することも特徴的です。これは急激な血清尿酸値の低下に伴う現象と考えられており、予防的にコルヒチン等の併用が推奨される場合があります。
使用成績調査では、以下の副作用が報告されています。
- 肝機能異常:0.90%(39例)
- 痛風性関節炎:0.79%(34例)
- そう痒症:0.35%(15例)
- 腎機能障害:0.35%(15例)
トピロキソスタットと他の薬剤との相互作用
トピロキソスタットは他の薬剤と併用する際に、特定の相互作用に注意が必要です。特に、XOR阻害作用を介した薬物代謝への影響から、いくつかの重要な禁忌・注意事項が存在します。
絶対的な併用禁忌薬剤:
- メルカプトプリン水和物:抗がん剤・免疫抑制剤として使用されるこの薬剤は、XORにより代謝されるため、トピロキソスタットとの併用によりメルカプトプリンの血中濃度が上昇し、重篤な副作用(骨髄抑制など)のリスクが高まります。
- アザチオプリン:免疫抑制剤であるアザチオプリンは体内でメルカプトプリンに代謝されるため、同様の理由で併用禁忌とされています。
- ビダラビン:抗ウイルス薬であるビダラビンは、XORにより代謝されるため、トピロキソスタットとの併用により幻覚、振戦、神経障害などのビダラビンの副作用が増強される可能性があります。
これらの薬剤とトピロキソスタットを併用する場合、薬物の血中濃度が上昇し、重篤な副作用が発現するリスクが高まるため、絶対に避けるべきです。処方前には患者の服用中の薬剤を十分に確認することが重要です。
その他の相互作用に注意すべき薬剤:
- ワルファリン:トピロキソスタットとの併用によりワルファリンの効果が増強される可能性があり、PT-INR値の定期的なモニタリングが必要です。
- テオフィリン:XORはテオフィリンの代謝にも関与するため、トピロキソスタットとの併用によりテオフィリンの血中濃度が上昇する可能性があります。
- 非ステロイド性抗炎症薬(NSAIDs):高尿酸血症患者では腎機能低下を伴う場合が多く、NSAIDsとトピロキソスタットの併用により腎機能への負担が増加する可能性があります。
これらの相互作用は理論的に考えられるものであり、実臨床での注意深いモニタリングが必要です。特に高齢者や腎機能低下患者では、相互作用のリスクが高まることがあるため、より慎重な投与が求められます。
トピロキソスタットの臨床試験から見る有効性
トピロキソスタットの有効性は複数の臨床試験で検証されており、血清尿酸値の低下効果と長期的な安全性が確認されています。以下に主な臨床試験の結果をまとめます。
国内第II相試験:
トピロキソスタット120mg/日および160mg/日の投与群では、用量依存的な血清尿酸値の低下効果が認められました。痛風関節炎を含む副作用発現頻度は120mg/日群で20.5%(8/39例)、160mg/日群で17.5%(7/40例)でした。主な副作用は、120mg/日群では痛風関節炎(5.1%)、四肢不快感(5.1%)、160mg/日群ではALT増加(7.5%)、AST増加(7.5%)、痛風関節炎(5.0%)であり、比較的良好な安全性プロファイルを示しています。
国内第III相試験(アロプリノール対照):
痛風を含む高尿酸血症患者206例を対象とした二重盲検並行群間比較試験では、トピロキソスタットを段階的に増量(40mg/日→80mg/日→120mg/日)し、16週間投与しました。その結果、アロプリノールと同等の尿酸値低下効果を示しつつ、腎機能低下患者においてもより安定した効果を発揮する傾向が認められました。副作用発現率は高かったものの(ALT増加12.0%、痛風関節炎11.0%など)、重篤なものは少なく、忍容性は良好でした。
長期投与試験(国内第III相試験):
121例の痛風・高尿酸血症患者を対象とした長期投与試験では、トピロキソスタットの長期的な安全性と有効性が検討されました。痛風関節炎の有害事象発現率は9.1%(11/121例)でした。副作用発現頻度は67.8%(82/121例)と高かったものの、多くは臨床検査値異常であり、臨床的に重要な有害事象は少なくなっています。特に注目すべきは、投与開始から血清尿酸値が安定的に低下し、長期間にわたり効果が持続したことです。
プラセボ対照比較試験:
プラセボ群との比較試験では、トピロキソスタット投与群で有意な血清尿酸値の低下が認められました。痛風関節炎の有害事象発現率は、本剤群で14.5%(9/62例)、プラセボ群で8.3%(5/60例)でした。副作用発現頻度は40.3%(25/62例)で、主な副作用は痛風関節炎14.5%(9/62例)、ALT増加9.7%(6/62例)、AST増加8.1%(5/62例)でした。
これらの臨床試験結果から、トピロキソスタットは高尿酸血症患者の血清尿酸値を効果的に低下させ、長期使用においても安定した効果を示すことが確認されています。特に従来のアロプリノールと比較して、腎機能低下患者でも用量調整の必要性が少ない点は臨床的に重要な特徴と言えるでしょう。
トピロキソスタットの特殊な患者群での使用上の注意点
トピロキソスタットは広く使用される高尿酸血症治療薬ですが、特定の患者群においては特別な注意が必要です。これらの患者群での使用経験は限られているため、リスクとベネフィットを慎重に評価する必要があります。
腎機能障害患者での使用:
腎機能障害患者におけるトピロキソスタットの使用は、特に注意が必要です。臨床試験では、尿中α1ミクログロブリン増加(27.3%)、β2ミクログロブリン増加(20.7%)、尿中アルブミン陽性(6.6%)などの腎関連マーカーの変動が高頻度に認められています。一方で、アロプリノールと比較して、中等度腎機能障害患者(eGFR 30-60mL/min/1.73m²)での用量調整の必要性が少ない特徴があります。
腎機能障害患者への投与では、以下の点に注意が必要です。
肝機能障害患者での使用:
トピロキソスタットの主な副作用として肝機能障害(2.9%)が報告されており、肝機能障害を有する患者では特に慎重な投与が求められます。市販後調査でも肝機能異常は最も多い副作用(0.90%)として報告されています。
肝機能障害患者への投与では、以下の点に注意が必要です。
- 投与開始前および投与開始後2-4週間のAST/ALT等の肝機能検査
- 異常値の上昇が認められた場合の投与中止
- 黄疸、倦怠感、食欲不振等の症状出現時の速やかな受診指導
- ウイルス性肝炎患者では肝炎の悪化に注意
高齢者への投与:
高齢患者では、腎機能や肝機能の低下が潜在していることが多く、副作用が発現しやすい可能性があります。高齢者特有の問題として、複数の合併症に対する多剤併用によるリスクも考慮する必要があります。
高齢者への投与では、以下の点に注意が必要です。
- 低用量からの開始と慎重な増量
- より頻回な臨床検査によるモニタリング
- 多剤併用による相互作用の可能性への注意
- 脱水や発熱時の一時的な投与中止の検討
妊婦・授乳婦への投与:
妊婦または妊娠している可能性のある女性に対するトピロキソスタットの安全性は確立していません。動物実験(ラット、ウサギ)では、催奇形性は認められていませんが、ヒトでの安全性データは不十分です。
妊婦・授乳婦への投与では、以下の点に注意が必要です。
- 妊娠が判明した場合は直ちに投与中止を検討
- 有益性が危険性を上回ると判断される場合のみ投与
- 授乳中は投与を避けるか、授乳を中止
- 妊娠可能年齢の女性には適切な避妊指導
これらの特殊な患者群では、トピロキソスタットの有効性と安全性のバランスを個々の患者ごとに慎重に評価し、適切な投与計画とモニタリングを行うことが重要です。特に併用薬の確認、定期的な臨床検査、患者教育を通じて、安全かつ効果的な治療を提供することが求められます。
部下をもったらいちばん最初に読む伝え方の本