テリパラチド 副作用と効果について
テリパラチドの作用機序と骨形成促進効果
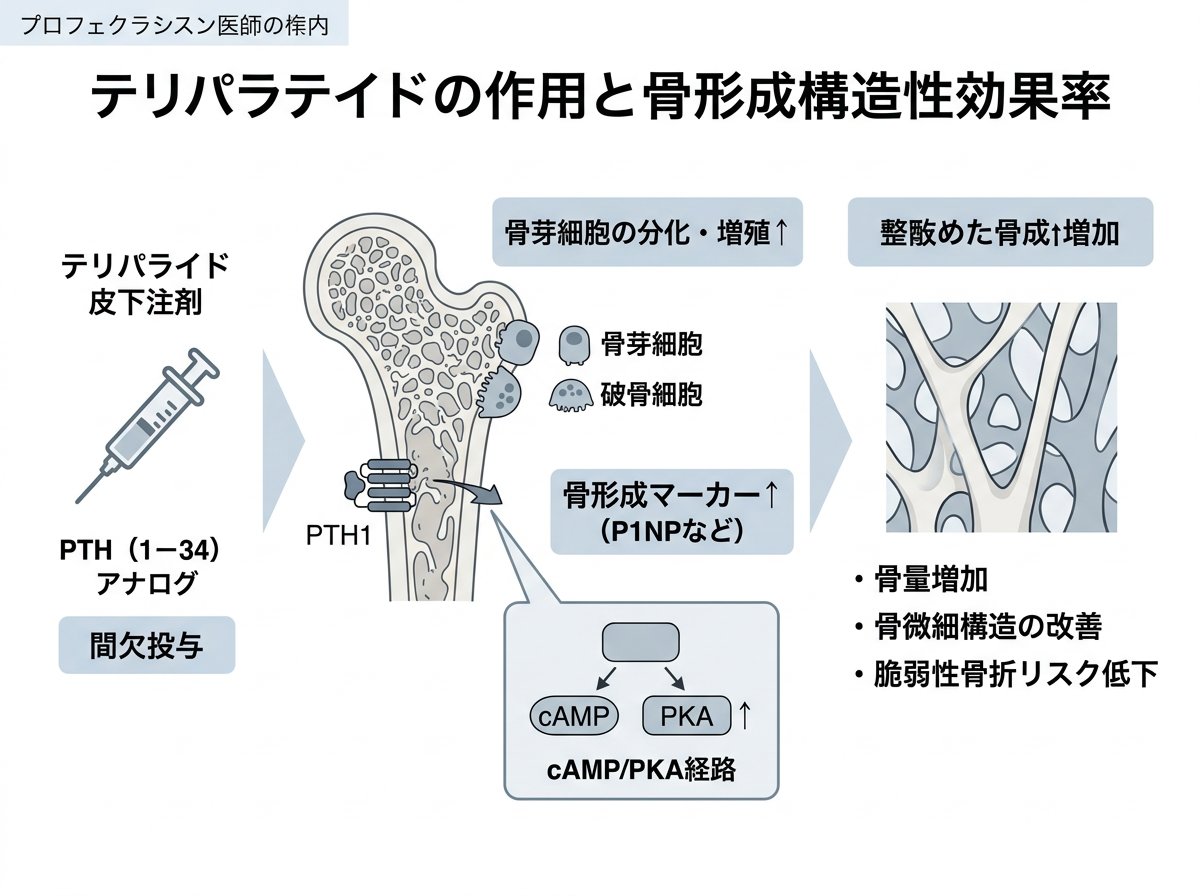
テリパラチドは、ヒト副甲状腺ホルモン(PTH)の活性フラグメントである1-34アミノ酸配列を有する合成ペプチドです。従来の骨粗鬆症治療薬と異なり、テリパラチドは骨吸収を抑制するのではなく、積極的に骨形成を促進する作用を持っています。
テリパラチドの骨代謝における主要な作用機序として、以下の点が重要です。
- 骨芽細胞の直接活性化:骨芽細胞表面のPTH受容体と結合することで、骨形成に必要な遺伝子発現を促進します。
- 骨細胞のアポトーシス抑制:骨の感覚細胞である骨細胞の生存期間を延長することで、骨強度の維持に貢献します。
- Wntシグナル経路の活性化:骨形成を促進する重要な細胞内シグナル伝達経路を活性化します。
テリパラチドの興味深い特徴として、投与方法により効果が大きく変わる「投与間欠性」があります。毎日一定時間に投与することで骨形成を促進しますが、持続的な投与では骨吸収も促進してしまうため、臨床使用では間欠投与が採用されています。
骨密度上昇効果は特に海綿骨に顕著であり、投与開始後3~6ヶ月で腰椎骨密度が平均6~8%上昇することが臨床試験で確認されています。これは他の骨粗鬆症治療薬と比較しても非常に高い効果です。
テリパラチド投与に伴う一般的な副作用と発現頻度
テリパラチドの治療開始後、約15%の患者が何らかの副作用を経験するとされています。日本骨代謝学会による3,500名を対象とした大規模調査結果から、副作用の発現パターンと頻度について詳細に把握することができます。
主な副作用とその発現頻度は以下の通りです。
| 副作用症状 | 発現頻度 | 好発時期 | 持続期間 |
|---|---|---|---|
| 悪心・嘔吐 | 8.2% | 投与直後 | 2-3時間 |
| めまい | 7.5% | 30分以内 | 1-2時間 |
| 頭痛 | 6.8% | 不定期 | 数時間 |
| 注射部位反応 | 4.3% | 投与時 | 1-2日 |
副作用の発現パターンとして重要なのは、投与開始から2週間以内に出現する初期症状として悪心や嘔吐、めまい、頭痛などがあることです。これらの初期症状は投与時刻の調整や投与速度の最適化により軽減できることが多いため、患者指導が重要です。
電解質異常に関する副作用としては、高カルシウム血症と高カルシウム尿症が高頻度で発現します。特に高カルシウム血症は、テリパラチドのPTH様作用の直接的な結果として生じるため、定期的な血清カルシウム値のモニタリングが必須です。
また、頻度は低いものの注意すべき重大な副作用として、以下が挙げられます。
- アナフィラキシー(頻度不明):呼吸困難、血圧低下、発疹などの症状
- ショック、意識消失(頻度不明):一過性の急激な血圧低下に伴う意識消失
血清カルシウム値が11.5mg/dL以上に上昇した場合や重篤な副作用が発現した際には、直ちに投与を中止する判断が求められます。
テリパラチドの骨折予防効果と臨床エビデンス
テリパラチドの骨折予防効果は複数の大規模臨床試験で実証されており、特に高リスク患者における二次予防に高い有効性を示しています。
最も重要な臨床エビデンスとして、椎体骨折の既往のある閉経後女性を対象としたFRT試験があります。この試験ではプラセボと比較して椎体骨折、非椎体骨折(大腿骨骨折を含む)を有意に減少させました。カプランマイヤー曲線の解析から、骨折予防効果は投与開始後約12ヶ月から明確になることが示されています。
テリパラチドの骨折リスク減少率は以下のとおりです。
- 新規椎体骨折:約65%減少
- 非椎体骨折:約53%減少
- 臨床的骨折全体:約45%減少
ただし、こうした効果が現れるまでには一定の期間が必要であり、ビスホスホネート製剤と同様に即効性はありません。効果発現までに約12ヶ月を要することを理解した上での治療計画が重要です。
また、テリパラチドには骨密度増加だけでなく、骨微細構造の改善効果もあることが高分解能CT研究で明らかになっています。具体的には。
- 海綿骨の骨梁数増加
- 骨梁構造の連結性向上
- 皮質骨の厚みと強度増加
これらの構造的改善は、単なる骨密度測定では評価できない骨質向上に貢献していると考えられています。
さらに、臨床的な付加価値として骨折後の疼痛軽減効果も報告されており、骨折治癒促進との関連が示唆されています。
テリパラチド治療における禁忌と注意事項
テリパラチド投与においては、適切な患者選択と慎重な経過観察が極めて重要です。以下の状態や既往歴のある患者ではテリパラチドの使用を避けるべきとされています。
特に重要な注意点として、長期投与によるがんリスクの問題があります。テリパラチドの非臨床試験(ラットのがん原性試験)において、投与量および投与期間に依存して骨肉腫を含む骨腫瘍性病変の発生頻度が増加することが報告されています。このリスクを考慮し、各製剤には使用期間の制限が設けられています。
また、テリパラチド治療を中止すると骨密度が速やかに低下し、治療前の状態に戻ってしまうという特性があるため、後療法が必須となります。一般的には、テリパラチド終了後にビスホスホネート製剤やデノスマブなどの骨吸収抑制薬による維持療法が推奨されています。
投与中のモニタリング基準としては、以下のパラメータの定期的な測定が推奨されます。
| 検査項目 | 測定頻度 | 中止基準 | フォロー間隔 |
|---|---|---|---|
| 血清Ca値 | 月1回 | >11.5mg/dL | 週2回 |
| 腎機能 | 3ヶ月毎 | eGFR<25 | 週1回 |
| 骨代謝マーカー | 6ヶ月毎 | ALP>600 | 2週間毎 |
臨床経過に応じて測定頻度を調整することも重要です。
テリパラチドとバイオシミラー製剤の安全性と経済効果
近年、テリパラチドのバイオシミラー製剤が開発され、臨床導入が進んでいます。バイオシミラーとは、既に承認されたバイオ医薬品(先行バイオ医薬品)と同等/同質の品質、安全性、有効性を有する医薬品として開発された後続品を指します。
テリパラチドのバイオシミラーに関して、医療経済学的観点から注目すべき点は薬剤費削減効果です。先行バイオ医薬品と比較して約30%の薬剤費削減が期待でき、医療費の適正化に貢献します。
しかし、バイオシミラーへの切り替えに際しては安全性の確保が最優先事項となります。国内の調査研究では、テリパラチドのバイオ先行品からバイオシミラーへ切り替えた症例において、副作用プロファイルに大きな差異は認められないことが報告されています。
テリパラチドバイオシミラーでも先行品と同様に、以下の副作用に注意が必要です。
- 頻度の高い副作用(1~5%):起立性低血圧、めまい、悪心、上腹部痛、頭痛、ALP上昇、血清クレアチニン値上昇、血中尿酸値上昇、血中尿素上昇
- より低頻度の副作用(1%未満):血中カリウム上昇、白血球数増加、肝機能異常(AST上昇、ALT上昇、γ-GTP上昇)
- 頻度不明の副作用:高カルシウム血症
バイオシミラー製剤を使用する際の患者教育ポイントとしては、先行品と同等の効果が期待できること、安全性プロファイルも同様であることを丁寧に説明することが信頼関係構築に重要です。また、薬剤費削減による経済的負担軽減のメリットも患者に理解してもらうことで治療アドヒアランスの向上が期待できます。
医療機関側のメリットとしては、薬剤費削減による医療経済効率の向上だけでなく、より多くの高リスク骨粗鬆症患者にテリパラチド治療を提供できる可能性が広がる点が挙げられます。
テリパラチドと他の骨粗鬆症治療薬の併用効果と相互作用
テリパラチドは骨形成促進作用を持つため、骨吸収抑制薬との併用療法については慎重な検討が必要です。臨床研究からは、特定の併用パターンにおいて相互作用による治療効果の減弱や予期せぬ副作用の発現が報告されています。
主要な骨粗鬆症治療薬との併用に関する注意点は以下の通りです。
| 薬剤分類 | 併用制限の理由 | 推奨休薬期間 | 骨密度への影響 |
|---|---|---|---|
| ビスホスホネート | 効果相殺 | 6ヶ月以上 | -2.7%/年 |
| SERM | 骨代謝への影響 | 3ヶ月以上 | -1.8%/年 |
| デノスマブ | 作用機序の重複 | 6ヶ月以上 | -3.2%/年 |
特にビスホスホネート製剤との併用では、骨形成マーカーであるP1NPが平均42%低下することが報告されています。また、骨密度の増加率が単独投与時の約60%まで低下するという結果が3,000例以上の大規模臨床試験で確認されています。
一方で、テリパラチドの治療後(投与期間満了後)のシークエンシャル療法(継続療法)としては、ビスホスホネート製剤やデノスマブなどの骨吸収抑制薬による治療が推奨されます。これはテリパラチド中止後の急速な骨密度低下を防ぐために必須のアプローチです。
また、薬剤相互作用としてはジギタリス製剤との併用に注意が必要です。テリパラチドにより血清カルシウム値が上昇すると、ジギタリスの作用が増強される可能性があります。
テリパラチド治療の最適化において重要なのは、個々の患者の骨折リスク、既往薬剤への反応性、併存疾患などを総合的に評価した上で、適切な治療シークエンスを設計することです。高齢者や複数の骨折リスク因子を有する患者では、テリパラチドによる初期治療後に骨吸収抑制薬による長期維持療法を組み合わせる戦略が骨折予防に最も効果的とされています。
近年の研究では、テリパラチドの間欠投与とデノスマブの併用療法(交互療法)が、それぞれの単独療法よりも優れた骨密度増加効果を示す可能性が報告されています。この新たな治療アプローチは、特に超高リスク患者に対する選択肢として注目されています。
世界は私たちのために作られていない