免疫チェックポイント阻害薬の種類と一覧
免疫チェックポイント阻害薬の抗PD-1抗体製剤の特徴
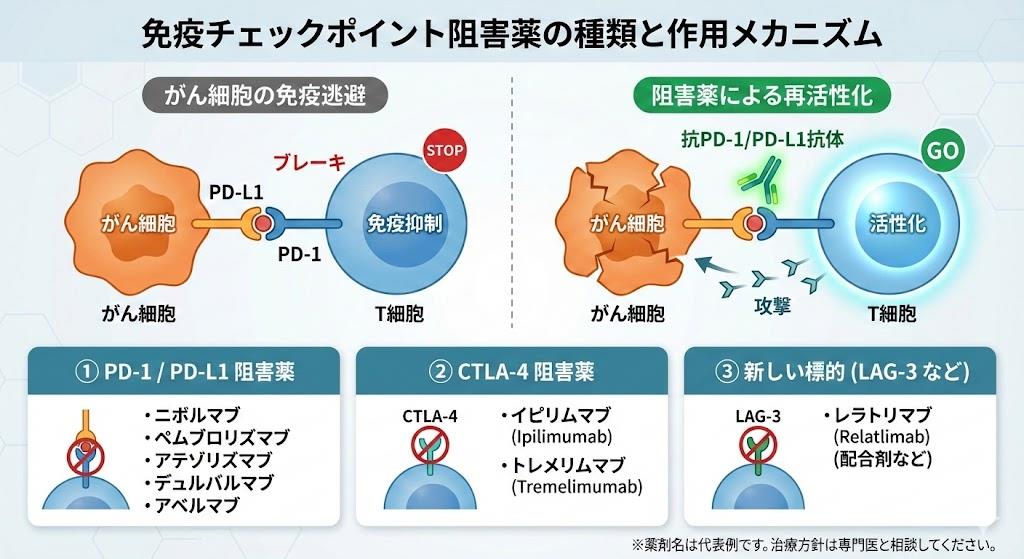
抗PD-1抗体は現在、日本国内で最も多く使用されている免疫チェックポイント阻害薬です。T細胞表面に存在するPD-1受容体を標的とし、がん細胞が発現するPD-L1との結合を阻害することで、がん細胞に対する免疫攻撃を再活性化させます。
ニボルマブ(オプジーボ)
小野薬品工業が開発し、2014年7月に世界初の免疫チェックポイント阻害薬として悪性黒色腫で承認されました。その後、適応は急速に拡大し、現在では以下の疾患で使用可能です。
薬価は規格により異なり、20mg製剤で27,130円/瓶、240mg製剤で311,444円/瓶となっています。オプジーボの特徴として、従来の抗がん剤治療後の二次治療として高い効果を示すことが挙げられます。
ペムブロリズマブ(キイトルーダ)
MSDが開発した抗PD-1抗体で、2016年9月に悪性黒色腫で承認されました。100mg製剤の薬価は214,498円/瓶です。キイトルーダの最大の特徴は、PD-L1発現率50%以上の非小細胞肺がんにおいて、一次治療から使用可能な点です。これにより、従来の化学療法による副作用を回避しながら治療を開始できる可能性があります。
セミプリマブ(リブタヨ)
サノフィが開発した比較的新しい抗PD-1抗体で、2022年12月に子宮頸がんの二次治療で承認されました。350mg製剤の薬価は450,437円/瓶と高額に設定されています。
免疫チェックポイント阻害薬の抗PD-L1抗体製剤の詳細
抗PD-L1抗体は、がん細胞側のPD-L1分子を直接標的とする免疫チェックポイント阻害薬です。抗PD-1抗体と類似の作用機序を持ちますが、標的分子が異なることで、若干異なる効果プロファイルを示します。
アテゾリズマブ(テセントリク)
中外製薬が販売する抗PD-L1抗体で、2018年1月に非小細胞肺がんの二次治療で承認されました。薬価は840mg製剤で445,699円/瓶、1200mg製剤で563,917円/瓶となっています。テセントリクは特に乳がん領域での開発が進んでおり、トリプルネガティブ乳がんに対する有効性が期待されています。
デュルバルマブ(イミフィンジ)
アストラゼネカが開発した抗PD-L1抗体で、2018年8月にステージ3非小細胞肺がんで承認されました。この薬剤の特徴は、根治的化学放射線療法後の維持療法として使用される点です。薬価は120mg製剤で67,871円/瓶、500mg製剤で275,693円/瓶と、他の免疫チェックポイント阻害薬と比較して比較的低く設定されています。
アベルマブ(バベンチオ)
メルクセローノが開発した抗PD-L1抗体で、2017年9月にメルケル細胞がんで承認されました。200mg製剤の薬価は166,397円/瓶です。メルケル細胞がんは希少がんの一つですが、アベルマブにより治療選択肢が広がりました。
免疫チェックポイント阻害薬の抗CTLA-4抗体の位置づけ
抗CTLA-4抗体は、T細胞の活性化初期段階において重要な役割を果たす免疫チェックポイント阻害薬です。CTLA-4は抗原提示細胞からの共刺激シグナルを阻害することで、T細胞の過度な活性化を防ぐ役割を担っています。
イピリムマブ(ヤーボイ)
ブリストル・マイヤーズスクイブが開発した世界初の抗CTLA-4抗体で、2015年8月に悪性黒色腫で承認されました。薬価は20mg製剤で170,598円/瓶、50mg製剤で419,578円/瓶となっています。イピリムマブの特徴として、単独使用よりも他の免疫チェックポイント阻害薬との併用で高い効果を示すことが挙げられます。
特に、ニボルマブとの併用療法は悪性黒色腫において標準治療の一つとなっており、単剤治療を上回る効果が確認されています。ただし、併用療法では重篤な免疫関連有害事象の発現率が高くなる傾向があるため、慎重な患者選択と副作用管理が必要です。
トレメリムマブ(イジュド)
アストラゼネカが開発した比較的新しい抗CTLA-4抗体で、2022年12月に承認されました。この薬剤の特徴は、デュルバルマブおよび化学療法との三剤併用で非小細胞肺がんに、デュルバルマブとの二剤併用で肝細胞がんに適応を持つ点です。薬価は25mg製剤で213,831円/瓶、300mg製剤で2,310,355円/瓶と設定されており、特に高用量製剤は極めて高額となっています。
免疫チェックポイント阻害薬の薬価と医療経済性の考察
免疫チェックポイント阻害薬の薬価は、がん治療における医療経済性の重要な課題となっています。単回投与あたりの薬剤費が数十万円に及ぶケースも多く、治療期間を考慮すると患者一人あたりの年間薬剤費は数百万円から一千万円を超える場合もあります。
薬価設定の背景
免疫チェックポイント阻害薬の高額な薬価設定には、以下の要因が関与しています。
- 新規作用機序による革新性の評価
- 開発コストの回収
- 既存治療法に対する優位性
- 希少疾病用医薬品としての側面
例えば、オプジーボは当初非常に高額な薬価が設定されましたが、適応拡大に伴い段階的な薬価引き下げが実施されています。これは、使用患者数の増加により医療保険財政への影響が懸念されたためです。
費用対効果の評価
免疫チェックポイント阻害薬の費用対効果を評価する際には、以下の要素を総合的に考慮する必要があります。
- 生存期間延長効果
- QOL(生活の質)の改善
- 長期寛解率
- 後発医薬品の登場による価格競争
- 併用療法による相乗効果
特に、一部の患者では長期間の寛解が得られるケースもあり、これらの患者では費用対効果が大幅に改善される可能性があります。
免疫チェックポイント阻害薬選択時の臨床的判断基準
臨床現場での免疫チェックポイント阻害薬の選択は、複数の要因を総合的に評価して行われます。単純に薬剤の種類だけでなく、患者の状態、がんの特性、治療歴など多角的な検討が必要です。
バイオマーカーに基づく選択
現在、免疫チェックポイント阻害薬の効果予測に最も重要なバイオマーカーはPD-L1発現率です。特に非小細胞肺がんにおいては。
- PD-L1発現率50%以上:ペムブロリズマブの一次治療適応
- PD-L1発現率1-49%:化学療法との併用を検討
- PD-L1発現率1%未満:化学療法を優先、二次治療で免疫チェックポイント阻害薬を検討
がん種別の選択指針
各がん種において、エビデンスレベルの高い免疫チェックポイント阻害薬が異なります。
- 悪性黒色腫:ニボルマブ単独またはイピリムマブとの併用
- 非小細胞肺がん:PD-L1発現率に応じてペムブロリズマブまたはニボルマブ
- 腎細胞がん:ニボルマブ単独または他の分子標的薬との併用
- 頭頚部がん:ニボルマブまたはペムブロリズマブ
副作用プロファイルによる選択
免疫チェックポイント阻害薬の副作用は従来の化学療法とは大きく異なり、免疫関連有害事象(irAE)と呼ばれる特徴的な副作用を示します。
これらの副作用の発現頻度や重症度は薬剤により異なるため、患者の既往歴や併存疾患を考慮した薬剤選択が重要です。
将来展望と新たな治療戦略
免疫チェックポイント阻害薬の分野では、現在も活発な研究開発が続いています。新たな免疫チェックポイント分子(LAG-3、TIM-3、TIGITなど)を標的とした薬剤の開発や、複数の免疫チェックポイント阻害薬の併用療法、さらには免疫細胞療法との組み合わせなど、様々な治療戦略が検討されています。
また、バイオマーカーの研究も進歩しており、PD-L1発現率以外にも腫瘍変異負荷(TMB)、マイクロサテライト不安定性(MSI)、HLA多様性などが効果予測因子として注目されています。これらの進歩により、将来的にはより精密で個別化された免疫療法が実現される可能性があります。
免疫チェックポイント阻害薬は、がん治療に革命的な変化をもたらした画期的な治療法です。適切な患者選択と薬剤選択により、従来の治療では困難であった進行がんに対しても良好な治療成績が期待できます。医療従事者として、これらの薬剤の特徴を十分に理解し、個々の患者に最適な治療選択を行うことが重要です。
免疫チェックポイント阻害薬 実践ガイドブック