抗リン脂質抗体症候群の症状と治療薬
抗リン脂質抗体症候群の主要症状と合併症
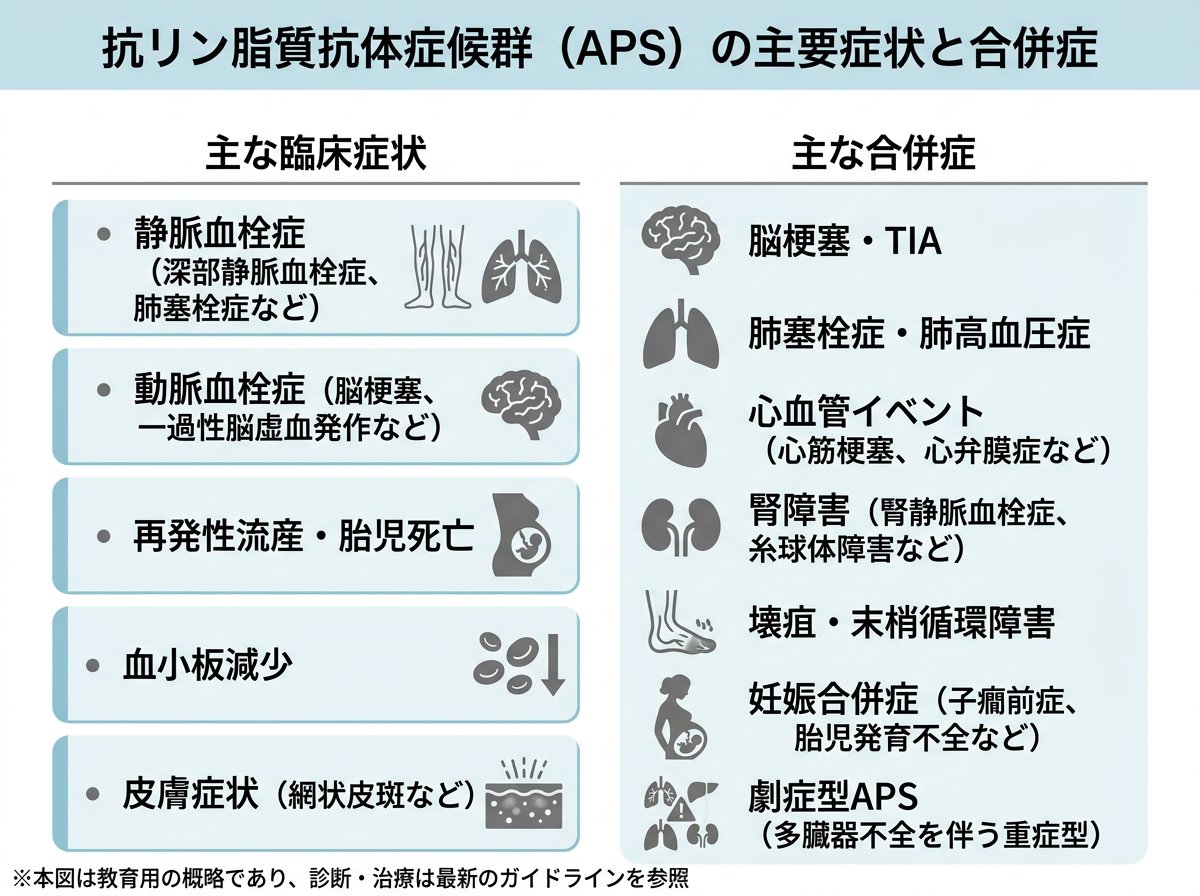
抗リン脂質抗体症候群(APS)は、抗リン脂質抗体という自己抗体が原因となって多彩な臨床症状を呈する疾患です。血栓症は全身のあらゆる部位で発生する可能性があり、症状の多様性がこの疾患の特徴といえます。
動脈血栓症の症状
動脈血栓症では脳梗塞が最も頻度が高く、APSにおける動脈血栓症の90%以上を占めます。若年性脳梗塞の原因として重要であり、特に明らかな危険因子がない場合にはAPSを疑う必要があります。脳梗塞による症状として、片麻痺、言語障害、意識障害、てんかん発作などが認められます。
興味深いことに、必ずしも画像上の梗塞病変を伴わない精神神経症状も報告されており、抗リン脂質抗体による直接的な神経障害の可能性も示唆されています。その他の動脈血栓症として、網膜動脈血栓症による視野障害や失明、心筋梗塞、腸間膜動脈血栓症、皮膚潰瘍などが挙げられます。
静脈血栓症の症状
静脈血栓症では下肢深部静脈血栓症が最も多く、下肢の腫脹、疼痛、熱感が主な症状です。これらの血栓が剥離して肺に到達すると肺血栓塞栓症を発症し、胸痛、呼吸困難、失神などの重篤な症状を呈する可能性があります。
海外の大規模コホート研究では、下肢深部静脈血栓症が32%、肺塞栓症が9%の頻度で認められており、これらの症状は生命に関わる可能性があるため迅速な診断と治療が求められます。
妊娠合併症と関連症状
APSの重要な特徴として妊娠合併症があります。妊娠中期(10週)以降の子宮内胎児死亡による習慣流産が特徴的で、胎盤の血流障害による胎盤機能不全が原因とされています。また、子宮内胎児発育遅延、妊娠高血圧症候群、子癇などの合併症も認められます。
その他の関連症状
血小板減少(22%)、網状皮斑(20%)、溶血性貧血(7%)なども高頻度で認められる症状です。網状皮斑は四肢に網目状の紫斑が出現する特徴的な皮膚症状で、APSの診断において重要な手がかりとなります。
抗リン脂質抗体症候群の診断基準と検査方法
APSの診断には、臨床基準と検査基準の両方を満たす必要があります。診断の精度を高めるため、検査は12週間以上の間隔をあけて2回以上陽性であることが条件となっています。
臨床基準
臨床基準には以下の項目が含まれます。
- 客観的に確認された血管血栓症(動脈、静脈、または小血管の血栓症)
- 妊娠合併症(10週以降の説明のつかない胎児死亡、34週未満の早産、習慣流産)
検査基準
検査基準として以下の3つの抗体検査が用いられます。
- ループスアンチコアグラント陽性
- 中等度以上の力価(40U/ml以上)のIgGまたはIgM型抗カルジオリピン抗体
- 中等度以上の力価(99パーセンタイル以上)のIgGまたはIgM型抗β2グリコプロテインI抗体
これらの検査のうち少なくとも1つが12週間以上の間隔をあけて2回以上陽性である必要があります。興味深いことに、梅毒の脂質抗体検査が偽陽性になることもあり、診断の際の注意点となります。
画像診断の重要性
血栓症の確定診断には画像検査が必要不可欠です。脳梗塞の診断にはMRI、肺塞栓症の診断には造影CT、下肢深部静脈血栓症の診断には超音波検査やCT静脈造影が用いられます。
劇症型APSの診断基準
稀ではありますが、劇症型抗リン脂質抗体症候群という重篤な病型も存在します。これは3つ以上の臓器に1週間以内に血栓症を発症し、組織病理学的に微小血栓を確認でき、抗リン脂質抗体陽性を示す病態です。
抗リン脂質抗体症候群の治療薬と薬物療法
APSの治療は抗血栓療法が中心となり、ステロイドや免疫抑制薬の有効性は証明されていません。治療選択は血栓症の部位と既往歴によって決定されます。
動脈血栓症に対する治療薬
動脈血栓症の既往がある場合、主に抗血小板療法が選択されます。第一選択薬として低用量アスピリン(バイアスピリン®100mg)1日1回が用いられます。
効果不十分な場合や再発リスクが高い症例では、異なる作用機序を有する抗血小板薬の併用が推奨されます。
重症例では抗血小板薬と抗凝固薬の併用、または強力な抗凝固療法(PT-INR 2.5-3.5)も検討されます。
静脈血栓症に対する治療薬
静脈血栓症の既往がある場合、抗凝固療法が選択されます。ワルファリンを用いてPT-INR 2.0-3.0を目標とした管理が標準的です。
近年では、直接経口抗凝固薬(DOAC)の使用も検討されていますが、APSにおけるエビデンスはまだ限定的であり、特に高リスク症例ではワルファリンが推奨されています。
一次予防における治療方針
血栓症の既往がなく抗リン脂質抗体陽性のみの場合、一次予防の適応は慎重に判断されます。ハイリスクの抗体陽性例(ループスアンチコアグラント陽性、または複数の抗体陽性)では、低用量アスピリンによる予防投与が検討されることがあります。
SLE合併例における特殊な治療
SLEに合併したAPSでは、ヒドロキシクロロキンが抗血栓予防効果を示すことが報告されており、併用療法として用いられることがあります。これは抗リン脂質抗体症候群特有の治療選択肢として注目されています。
抗リン脂質抗体症候群の妊娠時治療戦略
APSにおける妊娠合併症の管理は、母体と胎児の両方の安全性を考慮した専門的なアプローチが必要です。妊娠を希望するAPS患者や妊娠合併症の既往がある患者では、計画的な周産期管理が重要となります。
妊娠時の標準治療プロトコル
妊娠合併症の既往があるAPS患者が妊娠した場合、低用量アスピリン(81-100mg/日)に加えてヘパリンの投与が推奨されています。ヘパリンは胎盤を通過しないため、胎児への影響を最小限に抑えることができます。
具体的な治療スケジュール。
- 妊娠判明後速やかに低用量アスピリン開始
- 妊娠6-8週からヘパリン皮下注射開始
- 分娩直前までヘパリン継続
- 産後6-12週間の抗凝固療法継続
ヘパリンの種類と投与方法
未分画ヘパリンまたは低分子量ヘパリンが使用されます。低分子量ヘパリンは投与回数が少なく、血小板減少などの副作用リスクが低いため、近年では第一選択となっています。
妊娠中のモニタリング
妊娠中は定期的な胎児超音波検査による成長評価、胎盤機能の評価、母体の血小板数や凝固機能のモニタリングが重要です。妊娠高血圧症候群や子癇前症の早期発見にも注意を払う必要があります。
分娩時の管理
分娩時はヘパリンを一時中止し、分娩後早期に抗凝固療法を再開します。帝王切開が必要な場合は、適切な止血管理と血栓予防のバランスを取ることが重要です。
抗リン脂質抗体症候群の劇症型と緊急対応
劇症型抗リン脂質抗体症候群(CAPS: Catastrophic Antiphospholipid Syndrome)は、APSの中でも最も重篤な病型で、全APS患者の1%未満と稀ながら致死率が高い疾患です。医療従事者にとって迅速な認識と適切な初期対応が患者の予後を大きく左右する重要な病態です。
劇症型APSの診断基準
劇症型APSの確定診断には以下の4項目すべてを満たす必要があります。
- 3つ以上の臓器・系統の障害
- 症状が1週間以内に同時または連続して発症
- 組織病理学的に微小血栓の証明
- 抗リン脂質抗体陽性
臨床的特徴と発症機序
劇症型APSは感染症、外科手術、薬剤中止などを契機として発症することが多く、多臓器不全に至る急激な経過を辿ります。腎不全、呼吸不全、中枢神経症状、皮膚壊死、消化管出血などが同時多発的に発生し、播種性血管内凝固症候群(DIC)を合併することもあります。
緊急治療プロトコル
劇症型APSが疑われた場合、以下の集学的治療を迅速に開始する必要があります。
急性期治療
- ヘパリンの持続静脈内投与による強力な抗凝固療法
- ワルファリン導入による長期抗凝固療法の準備
- 副腎皮質ステロイド大量療法(メチルプレドニゾロン1000mg/日×3日間)
- 血漿交換療法による抗体除去
- 大量免疫グロブリン療法(0.4g/kg×5日間)
支持療法
新規治療薬への期待
難治性症例に対して、リツキシマブ(抗CD20モノクローナル抗体)やエクリズマブ(補体C5阻害薬)の有効性が症例レベルで報告されており、従来の治療に抵抗性を示す症例での治療選択肢として注目されています。
予後と長期管理
劇症型APSの生存率は約70%と報告されており、生存例では長期的な抗凝固療法の継続が必要です。再発率も高いため、定期的な外来フォローアップと患者教育が重要となります。
医療従事者は、APSの多様な臨床像を理解し、特に劇症型APSのような緊急性の高い病態を見逃さないよう、常に警戒心を持って診療にあたることが求められます。
難病情報センターの原発性抗リン脂質抗体症候群に関する詳細な疾患情報
日本リウマチ学会による抗リン脂質抗体症候群の症例解説
抗リン脂質抗体症候群 好酸球性多発血管炎性肉芽腫症 結節性多発動脈炎 2020